[anuncio_1]
Al confirmar el deterioro cognitivo antes de ordenar análisis de sangre amiloides, este enfoque de dos pasos reduce los falsos positivos, agiliza las derivaciones y acerca el diagnóstico de Alzheimer a las clínicas cotidianas.
Estudio: Detección de la enfermedad de Alzheimer en atención primaria mediante una prueba cognitiva digital autoadministrada y biomarcadores sanguíneos . Crédito de la imagen: Orawan Pattarawimonchai / Shutterstock
En un estudio reciente publicado en la revista Nature Medicine , investigadores de Suecia y Estados Unidos evaluaron si una breve batería cognitiva digital autoadministrada, sola o combinada con un panel de biomarcadores amiloides basados en sangre , detecta con mayor precisión el deterioro cognitivo y la enfermedad de Alzheimer (EA) clínica en atención primaria que la atención estándar.
Fondo
Uno de cada tres adultos mayores se preocupa por la pérdida de memoria; sin embargo, muchos nunca reciben un diagnóstico oportuno y preciso. La EA es la principal causa de demencia, impulsada por el depósito de beta-amiloide (Aβ), la agregación de tau y la neurodegeneración. Las etapas tempranas, como el deterioro cognitivo subjetivo (DCS) y el deterioro cognitivo leve (DCL), a menudo pasan desapercibidas en pruebas breves en papel como el Mini-Examen del Estado Mental (MMSE) o la Evaluación Cognitiva de Montreal (MoCA), especialmente en clínicas con atención urgente. El líquido cefalorraquídeo (LCR) o la tomografía por emisión de positrones (PET) de amiloide pueden confirmar la patología, pero estos métodos son invasivos, costosos o escasos. Los análisis de sangre como la tau 217 fosforilada (p-tau217) son prometedores; sin embargo, las probabilidades previas a la prueba varían ampliamente en atención primaria, con una positividad amiloide generalmente menor en DCS y mayor en DCL o demencia, lo que influye en el valor predictivo positivo (VPP). Las directrices internacionales enfatizan cada vez más los flujos de trabajo de dos pasos que confirman el deterioro antes de realizar las pruebas de biomarcadores. Investigaciones futuras deberían validar vías de primera línea eficientes, precisas y escalables.
Acerca del estudio
Los investigadores entrenaron y validaron BioCog, una batería de pruebas autoadministradas en tabletas, en dos cohortes suecas. Se utilizó una cohorte de atención secundaria del estudio BioFINDER-2 (ClinicalTrials.gov NCT03174938) para construir modelos de regresión logística y establecer puntos de corte; una cohorte independiente de atención primaria de 19 clínicas en el estudio BioFINDER-Atención Primaria (NCT06120361) sirvió para la validación externa. BioCog incluyó una lista de diez palabras (tres de recuerdo inmediato, recuerdo diferido y reconocimiento diferido), una tarea de velocidad de procesamiento cognitivo e ítems relacionados con la orientación temporal. El deterioro cognitivo objetivo se definió utilizando la Batería Repetible para la Evaluación del Estado Neuropsicológico (RBANS); en atención secundaria, se utilizó un indicador indirecto de la RBANS de pruebas neuropsicológicas similares.
La selección del modelo empleó la eliminación recursiva de características con el Criterio de Información de Akaike (AIC) y el área bajo la curva (AUC) de la característica operativa del receptor para el rendimiento. Se predefinieron esquemas de un punto de corte y de dos puntos de corte; este último creó una zona intermedia que se resolvería mediante una evaluación adicional. Se eligieron dos umbrales de probabilidad de BioCog (0,332 y 0,769) para alcanzar una sensibilidad y una especificidad del 95 %. Los médicos de atención primaria (PCP) realizaron evaluaciones estándar, que incluyeron MMSE, MoCA, tomografía computarizada y juicio clínico. Se probó un flujo de trabajo de dos pasos: el paso 1 involucró a BioCog para detectar el deterioro; el paso 2 involucró un panel de plasma (PrecivityAD2) que generó la Puntuación de Probabilidad Amiloide-2 (APS2) a partir de Aβ42, Aβ40, p-tau217 y no p-tau217. Los análisis de sensibilidad utilizaron la puntuación global de la Clasificación Clínica de Demencia (CDR) ≥0,5 como referencia de deterioro alternativa.
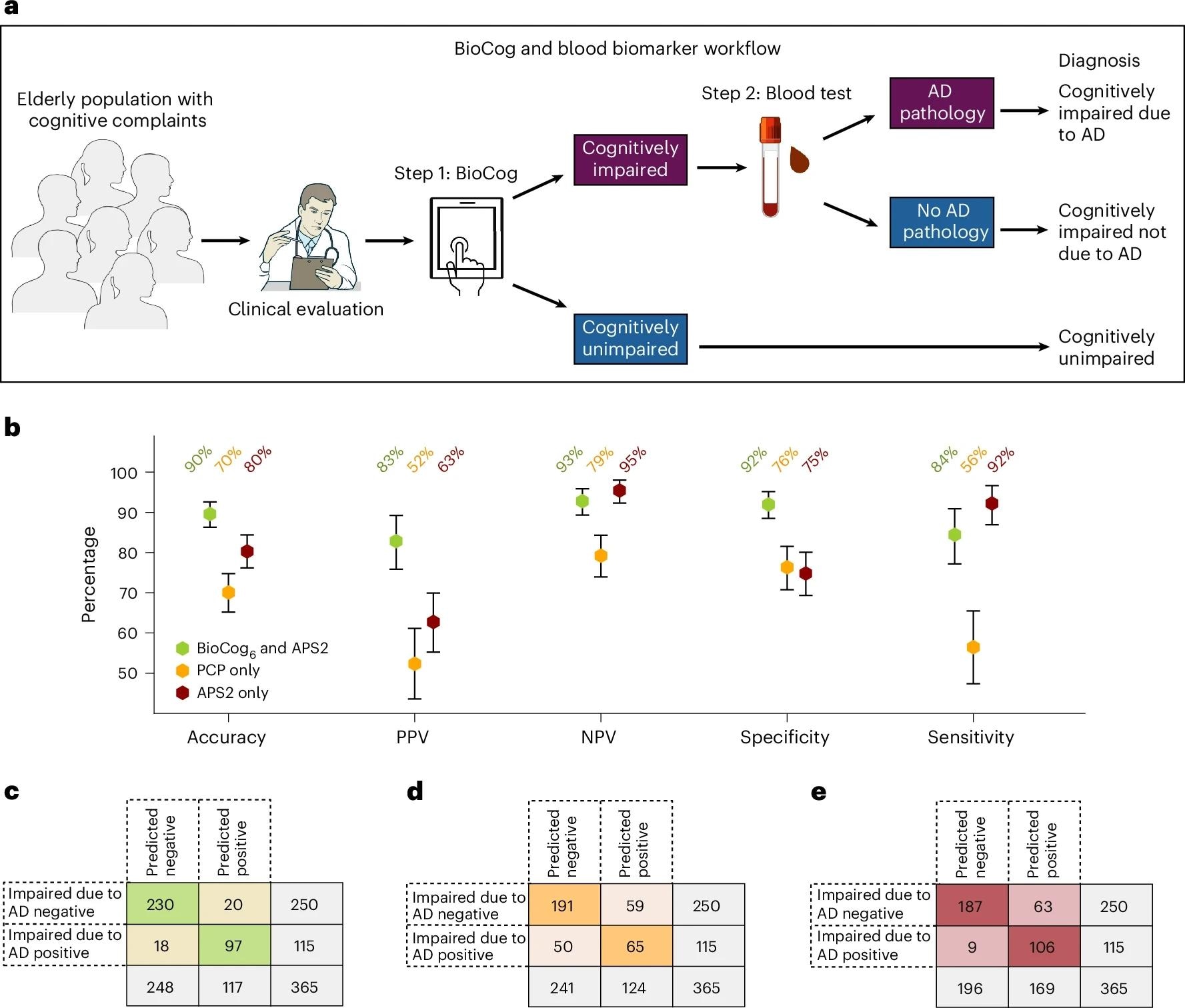
Comparación de un flujo de trabajo de diagnóstico basado en pruebas digitales y biomarcadores sanguíneos con la evaluación clínica estándar actual en la cohorte de atención primaria. Las comparaciones se realizaron en un subconjunto de individuos con todos los datos existentes disponibles (n = 365; consulte la Tabla complementaria 17 para obtener características detalladas de la población). a. Nuestro flujo de trabajo de atención primaria propuesto en dos pasos consiste en el paso 1, la detección del deterioro cognitivo mediante BioCog, seguido del paso 2, una evaluación de biomarcadores sanguíneos para evaluar si la patología de EA está presente en individuos con deterioro cognitivo. b , Evaluación del flujo de trabajo utilizando nuestro modelo BioCog 6 para el paso 1 y el biomarcador plasmático APS2 para el paso 2 (verde). El flujo de trabajo se comparó con una evaluación clínica estándar realizada por PCP en la que el médico evalúa si el paciente tenía deterioro cognitivo (DCL o demencia) y si el deterioro fue causado por EA (sin ningún biomarcador) (PCP AD , naranja), y con un flujo de trabajo que utiliza solo el biomarcador plasmático APS2 sin ninguna evaluación cognitiva (rojo). Las barras de error indican el IC del 95 %, y el punto central corresponde al valor medio. Crédito: Imágenes adaptadas de NIAID NIH BIOART ( https://bioart.niaid.nih.gov ).
Resultados del estudio
En atención secundaria (n=223; edad media de 73 años), el mejor modelo de seis variables (BioCog6: recuerdo diferido, velocidad de procesamiento correcta, rendimiento en el recuerdo inmediato, tiempo total, edad y reconocimiento diferido) alcanzó un AUC de 0,96 y una precisión del 89 % para el deterioro cognitivo verificado objetivamente con un único punto de corte. Un enfoque con dos puntos de corte alcanzó una precisión del 96 %, con un 18 % de participantes en una zona intermedia que requirió seguimiento. La psicometría respaldó la viabilidad y la validez: fuertes correlaciones convergentes con análogos en papel, correlaciones divergentes débiles con dominios no relacionados, un tiempo promedio de finalización de aproximadamente 11 minutos y solo alrededor del 2 % reportó dificultad con las instrucciones.
La validación externa en atención primaria (n = 403; edad media de 77 años) mostró un AUC de BioCog6 de 0,93 y una precisión del 85 % (valor predictivo positivo [VPP] del 87 %, valor predictivo negativo [VPN] del 83 %, sensibilidad del 88 %, especificidad del 82 %) utilizando un punto de corte, superando significativamente la evaluación del PCP (precisión del 73 %) basada en las pruebas e imágenes habituales. Con dos puntos de corte transferidos del entrenamiento, la precisión aumentó al 90 % (VPP del 91 %, VPN del 89 %) con un grupo intermedio del 18 %. Las comparaciones directas favorecieron a BioCog6 sobre el aprendizaje de asociaciones pareadas de MMSE, MoCA, Mini-Cog y la Batería Automatizada de Pruebas Neuropsicológicas de Cambridge (CANTAB), tanto en análisis de un punto de corte como, cuando estaban disponibles, en análisis de dos puntos de corte, incluso después de los ajustes demográficos.
Fundamentalmente, el flujo de trabajo de dos pasos adaptado para atención primaria (primero BioCog y luego solo análisis de sangre para aquellos con deterioro objetivo) identificó la EA clínica verificada por biomarcadores (deterioro debido a EA por consenso de expertos con apoyo de LCR o PET-Aβ) con una precisión del 90 % (VPP 83 %, VPN 93 %, especificidad 92 %, sensibilidad 84 %). Esto superó las vías solo para atención primaria (precisión 70 %) y superó a los análisis de sangre solos (precisión 80 %), que mostraron una tasa de falsos positivos aproximada del 17 % cuando se utilizaron sin un filtro de deterioro. El uso de dos puntos de corte tanto para BioCog como para APS2 elevó la precisión al 95 %, con una zona intermedia más amplia (aproximadamente 30 %), lo que enfatiza la compensación entre la certeza y las derivaciones indeterminadas. Los resultados fueron precisos al sustituir CDR ≥0,5 por RBANS (las métricas primarias disminuyeron modestamente pero se mantuvieron altas) y al eliminar la edad del modelo BioCog.
La interpretación se centra en la probabilidad preprueba: dado que solo las personas con deterioro cognitivo (no con anemia falciforme) son elegibles para las inmunoterapias dirigidas a Aβ implementadas recientemente, un filtro inicial eficiente que confirma el deterioro antes que los biomarcadores sanguíneos reduce los falsos positivos, mejora el VPP y se alinea con las recomendaciones internacionales y el perfil de producto preferido de la Organización Mundial de la Salud para análisis de sangre. La administración digital estandariza la administración, captura características de tiempo más allá de las puntuaciones brutas y minimiza el tiempo del personal, lo cual es una ventaja para las clínicas con alta demanda que enfrentan una demanda creciente. Sin embargo, los autores advierten que BioCog debe complementar, no reemplazar, el juicio clínico, y que aún se requiere la validación en otros idiomas, culturas y entornos longitudinales.
Conclusiones
Esta prueba de concepto demuestra que una batería cognitiva digital breve y autoadministrada puede identificar con precisión el deterioro cognitivo objetivo en atención primaria. Al complementarse con un panel de biomarcadores sanguíneos específicos, permite diagnosticar la EA clínica con una precisión considerablemente mayor que el estándar de atención actual. El enfoque gradual de “análisis y análisis de sangre” mejora la certeza diagnóstica, reduce las derivaciones inapropiadas y prioriza a los candidatos para terapias dirigidas al Aβ. Si bien la generalización más allá de los entornos suecos y su utilidad longitudinal requieren mayor estudio, la vía es práctica, escalable y coherente con las directrices internacionales: primero se confirma el deterioro y luego se utilizan biomarcadores sanguíneos para inferir la patología amiloide, lo que permite obtener diagnósticos más tempranos y fiables en las clínicas habituales.
Referencia de la revista:
- Tideman, P., Karlsson, L., Strandberg, O., Calling, S., Smith, R., Midlöv, P., Verghese, PB, Braunstein, J.B., Mattsson-Carlgren, N., Stomrud, E., Palmqvist, S. y Hansson, O. ( 2025 ). Detección de la enfermedad de Alzheimer en atención primaria mediante una prueba cognitiva digital autoadministrada y biomarcadores sanguíneos. Nat Med . DOI: 10.1038/s41591-025-03965-4, https://www.nature.com/articles/s41591-025-03965-4
[anuncio_2]